- 测序深度(depth): 指测序得到的总碱基数与待测基因组大小的比值。假设一个基因大小为2M,测序深度为10X,那么获得的总数据量 为20M。
- 覆盖度(coverage): 指测序获得的序列占整个基因组的比例。由于基因组中的高GC、重复序列等复杂结构的存在,测序最终拼接组装 获得的序列往往无法覆盖有所的区域,这部分没有获得的区域就称为Gap。例如一个细菌基因组测序,覆盖度是98 %,那么还有2%的序列区域是没有通过测序获得的。(你想实际测到的内容占想测内容的比例。)
外显子组测序(Exome-seq)
外显子组(Exome)是指真核生物基因组中全部外显子区域的总和,包含了蛋白质合成最直接的信息。
外显子组测序是指利用序列捕获或者靶向技术将全基因组外显子区域DNA富集后再进行高通量测序的基因组分析方法,是一种通过高通量测序发现与蛋白质功能变异相关遗传突变的一种基因组分析技术。外显子组包含约1%的基因组(约30MB,包含约180,000个外显子,22,000个基因),却包含约85%的致病突变,与个体表型相关的大部分功能性变异也都集中在染色体的外显子区。对于试图揭示超过6,800种罕见疾病原因的遗传研究人员而言,外显子组测序能够识别单核苷酸变异体(SNVs)、小插入缺失(InDels)以及能够解释复杂遗传疾病的罕见的原发性突变。
与全基因组测序(WGS)相比,全外显子组测序(WES)费用更低、周期更短、覆盖度更深、数据准确性更高,更加简便、经济、高效。
与RNA-Seq的区别
-
测序范围的区别: 全外显子测序和转录组测序的测序范围是已知的,均针对基因组的转录区域进行测序,但它们有一定的差异,主要为:(1)使用范围有所不同。外显子组测序只能对已知基因组序列信息的物种进行测序,而转录组测序没有这样的限制。转录组可以对Non-coding RNA等进行测序,而外显子组测序仅限于外显子区域;(2)转录组可以反映特定时刻、特定组织该物种的基因表达情况,而外显子组测序不具备此能力。但是,因为部分基因低表达或组织特异表达,转录组难以获得物种全部外显子的信息,而外显子组测序不受表达情况影响,可均一地获得外显子区域序列信息;(3)从转录组获得的遗传信息可能受到转录后加工的影响而导致与基因组不符,而外显子测序无此影响。
-
测序深度的区别: 全外显子测序的测序深度在任何一个点是均匀的;转录组测序一定是不均匀的,以外显子为单位的不均匀
所需测序深度
外显子组测序的深度根据研究需要而定。例如,如希望检测的突变为种系突变(Germline Mutation)时,100×左右的测序深度则足以很好地覆盖外显子区域,获得较为准确的测序结果;而如希望检测的变异为体细胞突变(Somatic Mutation)时,考虑到检测样本(肿瘤组织、cfDNA)的异质性,则需150X甚至更高的测序深度才能够检测到这些变异。
外显子组捕获测序常用平台
目前主要有Illumina、Agilent、BGI、罗氏NimbleGen四家的外显子捕获试剂。NimbleGen和Illumina使用的是DNA探针;Agilent和BGI使用的是RNA探针。其中以基于液相探针杂交捕获技术的Agilent平台最常用。Agilent SureSelect Human All Exon V6人全外显子捕获系统采用120-mer的RNA作为“诱饵”探针,能够高效地捕获带有SNV,InDel等突变的基因组序列。
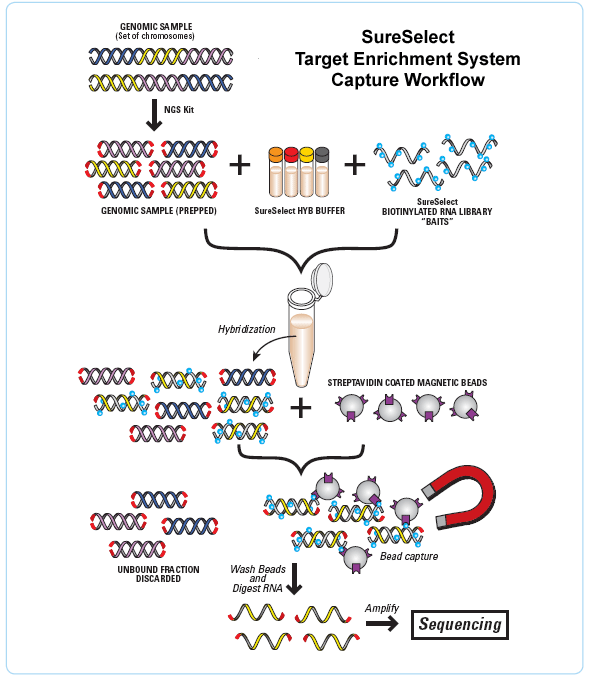
Aglient SureSelect外显子捕获系统
优势
针对与疾病最相关的蛋白质编码区域进行测序,发现影响蛋白结构功能变异相关的遗传突变;
测序深度更高,有利于发现常见变异、低频变异和罕见变异;
外显子捕获试剂盒选择丰富,高标准的建库上机流程,显著提高针对样品的使用效率。
分析流程
全外显子组测序-信息分析-肿瘤方向
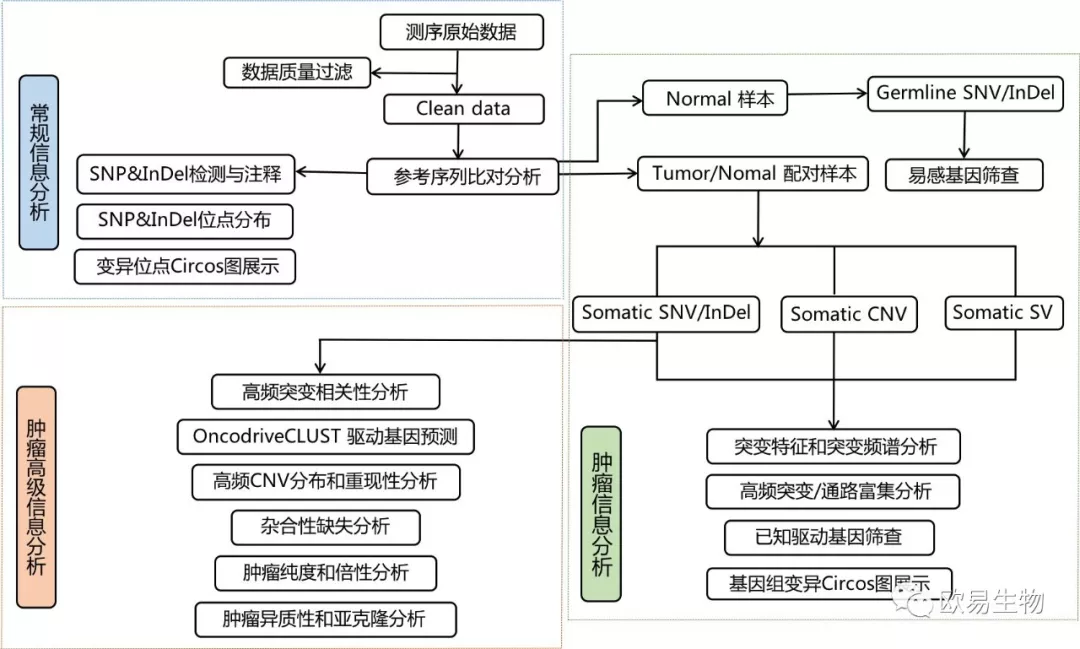
全外显子组测序-信息分析-遗传病方向
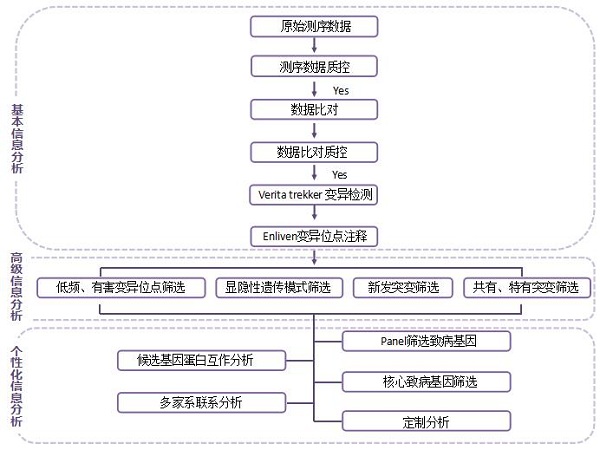
两个带脚本的分析流程: 肿瘤外显子全流程notes, 肿瘤全外显子测序数据分析流程大放送
WES在产前诊断方面面临的挑战
- 如何短时间内进行大量的数据分析与解读
- 如何识别低外显率和可变表现度的疾病
- 针对未知意义的变异(VOUS),如何提供准确的预测与遗传咨询
- WES不能检测非整倍体、多倍体、平衡易位、CNV等染色体异常
- 基因组部分区域,特别是GC富集区,WES难以有效覆盖,可能存在漏诊的状况
